每年氨的产量约为 200 兆吨。这使它成为世界上产量第二大的化学品,仅次于硫酸。有多种生产氨的方法,但 Haber-Bosch 工艺仍然是最普遍的工艺,约占总产量的 90%。Haber-Bosch 和其他工业规模生产过程需要高温(超过 400°C)和高压(超过 150 bar)。需要这些条件来破坏氮中的强键并与氢反应形成氨 (NH3)。
这些过程约占全球能源消耗的 1%,主要以化石燃料为基础。因此,氨是全球温室气体排放量最大的化学反应,约占全球 CO2排放总量的 1.5%。此外,预计未来几年对氨的需求只会增加——主要是因为它用于合成肥料以满足不断增长的全球人口,尽管它也被视为一种船用燃料。
气候方面以及能源和食品方面的主要挑战之一是氨的生产。今天,它是在世界上一些最大的工厂生产的。制造氨的唯一真正有效的方法是在高温高压下使用碳基原料。大自然非常擅长在环境压力和温度下在固氮酶等酶中制造氨。然而,该过程非常缓慢并且不可能扩大到工业生产。
——共同通讯作者 Tejs Vegge 教授,DTU Energy 和 VILLUM 可持续燃料和化学品科学中心 (V-Sustain)
Vegge教授与中国科学院大连化学物理研究所(DICP)的陈平教授共同领导了这项研究。
Tejs Vegge 和他在 DTU 的同事、Jaysree Pan 博士和 Heine A. Hansen 副教授与 DICP 的团队一起推出了一类新的复杂金属氢化物催化剂,可以在温和条件下合成氨。
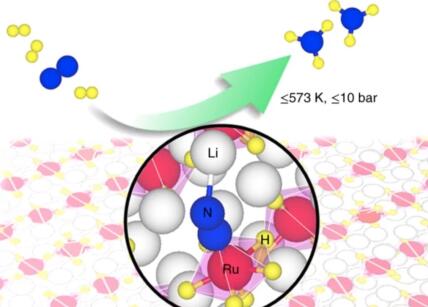
基于金属铁或钌的传统多相催化剂通过相对能源昂贵的途径介导二氮离解和氢化。在这里,我们报告了三元钌络合物氢化物 Li4RuH6和 Ba2RuH6作为替代类别的催化剂,由富电子和富氢 [RuH6] 阴离子中心组成,用于非离解二氮还原,其中氢化氢传输中心之间的电子和质子,以及 Li/Ba 阳离子稳定 NxHy(x = 0–2, y = 0–3) 中间体。三元复合氢化物的所有组分的动态和协同参与促进了具有窄能量跨度和多步过程的完美平衡动力学障碍的缔合反应机制,导致在温和条件下以优异的动力学从 N2 + H2生产氨.
——王等人。
他们的工艺使他们能够在低至 300 °C (573 K) 的温度和低至 1 bar 的压力下合成氨。这些催化剂的实际应用显示出基于可再生能源的小规模氨生产的前景。此类系统通常需要在约 50 bar 的压力和低于 400 °C 的温度下运行的催化剂。
我们相信我们的研究脱颖而出,因为这种新型催化剂实际上介于生物过程和工业过程之间。它有一些来自人类的人工过程——多相催化——以及一些来自酶促和均相催化的东西。这是一种全新的制造氨的方法,我们正在使用两全其美的方法,使我们能够显着降低温度和压力。
——维吉教授
氮的还原是通过多种氢化钌配合物 [RuH6]4- 实现的,这些配合物富含电子和氢。氢在中心和氮之间传输电子和质子。同时,碱金属锂或钡 (Li/Ba) 可稳定反应中间体。然而,这个过程是高度动态的;该综合体的几个部分还具有其他功能。仅计算就需要数年时间才能完成。
一切都与我们之前看到的不同。例如,尽管钌是氨催化中众所周知的成分,但它以不同的形式存在并且表现不同。它被氢原子包围并形成氢化物复合物,使其能够以一种新的方式转移氢。你可以把这个催化剂想象成一个交响乐团,每个部分都必须协同工作才能发挥作用。令人着迷的部分是它确实有效——没有错误的音符。
氨催化可以说是世界上研究最多的催化系统。作为一名科学家,找到一种真正的新机制来打开通往新世界的大门是非常令人满意的。然而,它也可能为以能源密集程度较低的方式生产氨开辟新的可能性。需要今天的大型工厂才能使生产有利可图。我们的催化剂或类似概念可以在较小的、分散的工厂中进行生产。这也将减少运输,这大大增加了当今氨的价格和 CO2排放量。
——维吉教授






